Att förstå betydelsen av kompressionsbehandling vid VTE-prevention
När vi får ett litet sår är vi tacksamma över blodets förmåga att koagulera för att skydda såret och förhindra ytterligare blodförlust. Men när blodet börjar koagulera på fel plats vid fel tidpunkt kan konsekvenserna förändra hela livet och till och med vara dödliga. Varje år orsakarblodproppar i de djupa venerna ett stort lidande för miljontals människor. I den här artikeln tar vi en närmare titt på blodproppar, varför de uppstår och hur Flowtron Active Compression System kan hjälpa till att förebygga dem.
”Uppskattningsvis drabbas tio miljoner personer om året av venös tromboembolism (VTE) globalt sett. Det är en livshotande sjukdom som kan innebära stora kostnader för akutvård och sjukvården”, säger Henrik Runnerström, Global Director för Product Category Management, VTE Prevention på Arjo.
Cirka 30 procent av patienterna dör inom 30 dagar efter att de utvecklat VTE, medan 25 procent av oväntade dödsfall hos inneliggande patienter diagnostiseras med lungemboli vid obduktion1.
Ungefär en tredjedel av patienter med djup ventrombos (DVT) får posttrombotiskt syndrom, en sjukdom som orsakar lidande, svullnad och värk1. För 25 procent av dessa patienter2 förknippas den resulterande kroniska sårbildningen med stora kostnader för den löpande behandlingen3.
Henrik fortsätter: ”Förutom det mänskliga lidandet medför det stora antalet VTE-fallen en betydande kostnadsbörda för akutvården och sjukvården.”
Vad är VTE?
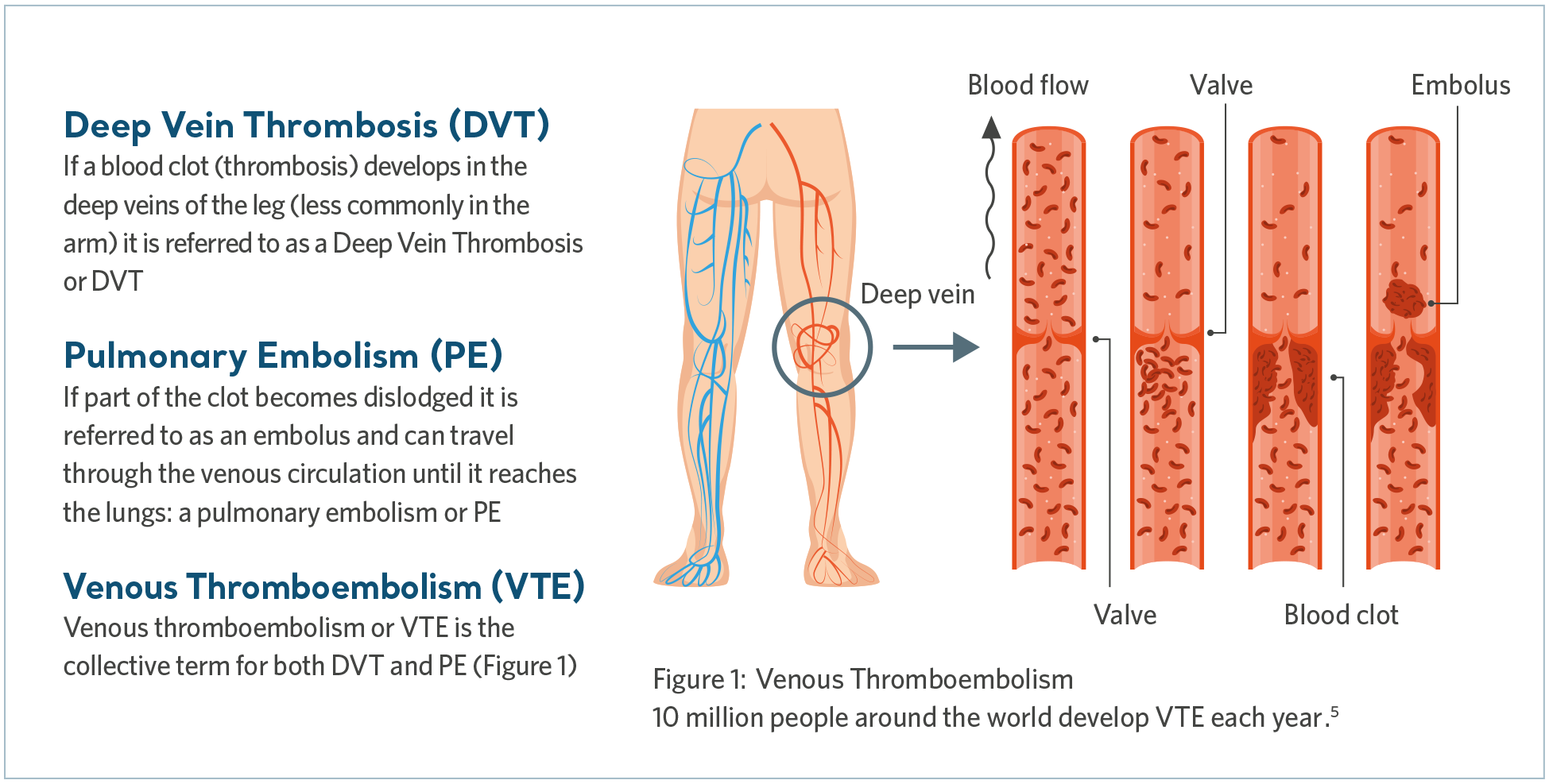
Venös tromboembolism (VTE) är ett samlingsbegreppet som innefattar djup ventrombos (DVT) och lungemboli (PE). DVT är när en blodpropp bildas i en djup ven, oftast i benet, medan lungemboli kan uppstå om blodproppen lossnar och transporteras till lungorna och blockerar en del av eller hela blodtillförseln.
Lungemboli är ett potentiellt dödligt tillstånd4. Vid tidig diagnos och behandling finns chansen att patienten återhämtar sig, men långsiktiga komplikationer kan innebära livslång behandling och kroniskt lidande för patienten.
Vad orsakar VTE?
VTE utlöses när flera riskfaktorer, som tillsammans kallas för ”Virchows triad”, påverkar homeostasen i kroppen och leder till koagulering.6 Låt oss titta på faktorerna som utgör Virchows triad:
Virchows triad
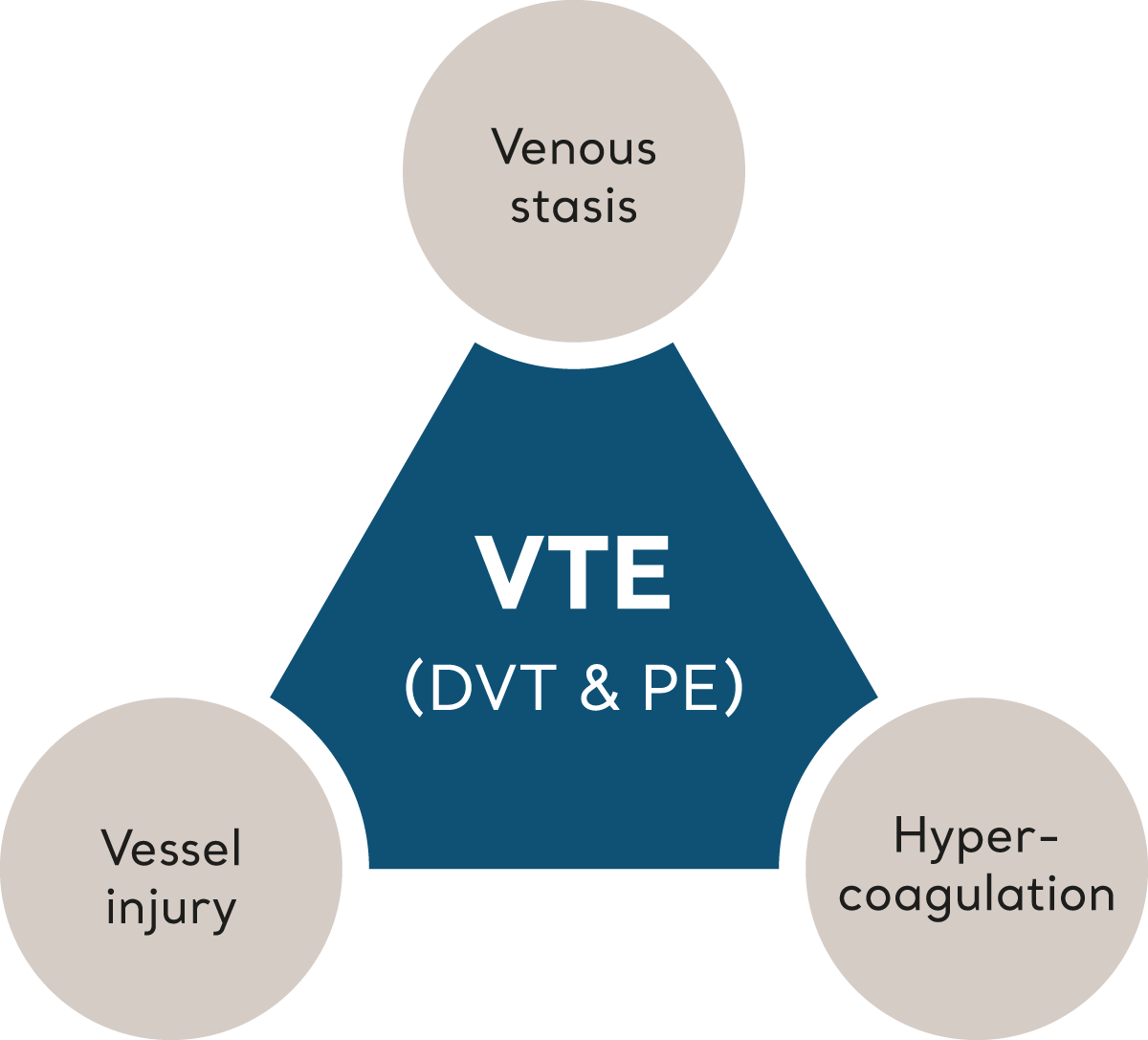
Venös stas
Omständigheter som gör att blodflödet saktar ner (stas) i de djupa venerna ökar risken för VTE. Orörlighet, kanske på grund av ålder, skörhet eller ordinerat sängliggande, är en tydlig riskfaktor.
Fysisk obstruktion av de djupa kärlen, antingen på grund av yttre krafter eller tryck från tumörer och lymfkörtlar, är också inblandad, liksom tidigare DVT.
Hyperkoagulation
Förändringar i bloddensitet och kemi kan öka risken för att blodet koagulerar. Detta är förknippat med tillstånd som vanlig dehydrering till hypoxi, malignitet, trauma, systemisk inflammatorisk sjukdom, genetisk predisposition och hormonbehandling.
Kärlskada
Skada kan inträffa genom oavsiktligt trauma eller genom medicinska ingrepp såsom kirurgiska eller invasiva ingrepp. När en skada inträffar initierar en normal fysiologisk serie av händelser som påverkar trombocyterna och eventuell bildning av en blodpropp. Denna skyddsmekanism försluter skadan och påbörjar läkningsprocessen. Ibland är denna process dock överdriven eller olämplig.
Vilka riskerar att drabbas?
Kirurgiska inneliggande patienter är en särskild riskgrupp7 eftersom kirurgi i sig själv ökar risken, på grund av anestesin (hyperkoagulabilitet), muskelavslappnande medel (stas) och det kirurgiska ingreppet
(kärlskada). Det är också tydligt att icke-kirurgiska sjukhuspatienter löper hög risk för VTE.
Henrik Runnerström säger: ”Det finns många faktorer som bidrar till VTE, och även om sjukdomen ofta är förknippad med sängliggande människor och äldre kan den också drabba en till synes frisk och atletisk person vid god hälsa.”
Den tidigare elithockeyspelaren Stefan Elvenes är ett exempel på detta. Några månader efter att han gick i pension från ishockey – efter en 22-årig karriär på högsta nivå i Sverige och Danmark – märkte han en svullnad i bakbenet på vänster ben.
”När läkaren sa att det var en blodpropp kunde jag inte tro det. Jag var bara 37 år och ändå i väldigt god form. Jag skulle inte kunna drabbas av något sådant”, säger Stefan.
Efter att ha fått höra att yngre och atletiska personer också kan få blodproppar fick Stefan en framgångsrik behandling med blodförtunnande medel. Men tre veckor efter att han slutade ta sin medicin fick han en allvarlig panikattack.
”I bakhuvudet fanns tanken, när jag slutar medicinera finns det en risk för att jag kan drabbas av en ny blodpropp. Det utlöste nog mina panikattacker”, säger Stefan. ”Jag var mentalt sett ett vrak under lång tid. Men regelbunden behandling hos en psykolog hjälpte mig att ta itu med rädslan. Idag är jag tillfreds med det.”
Förhindra VTE
Farmakologisk profylax som de blodförtunnande läkemedel Stefan behandlades med är ett sätt att behandla VTE. Preventionsstrategierna omfattar även olika mekaniska metoder, som Intermittent Pneumatic Compression (IPC) och graderade kompressionsstrumpor(GCS).
IPC är en mycket väl etablerad och bevisat effektiv intervention med övertygande evidens och få biverkningar - IPC är indikerat för inlagda patienter med många varierande förutsättningar som löper risk att drabbas av VTE.
Syftet med IPC är att förflytta blod från de djupare venerna genom intermittent uppblåsning och tömning av en manschett som är ansluten till en elektrisk pump.
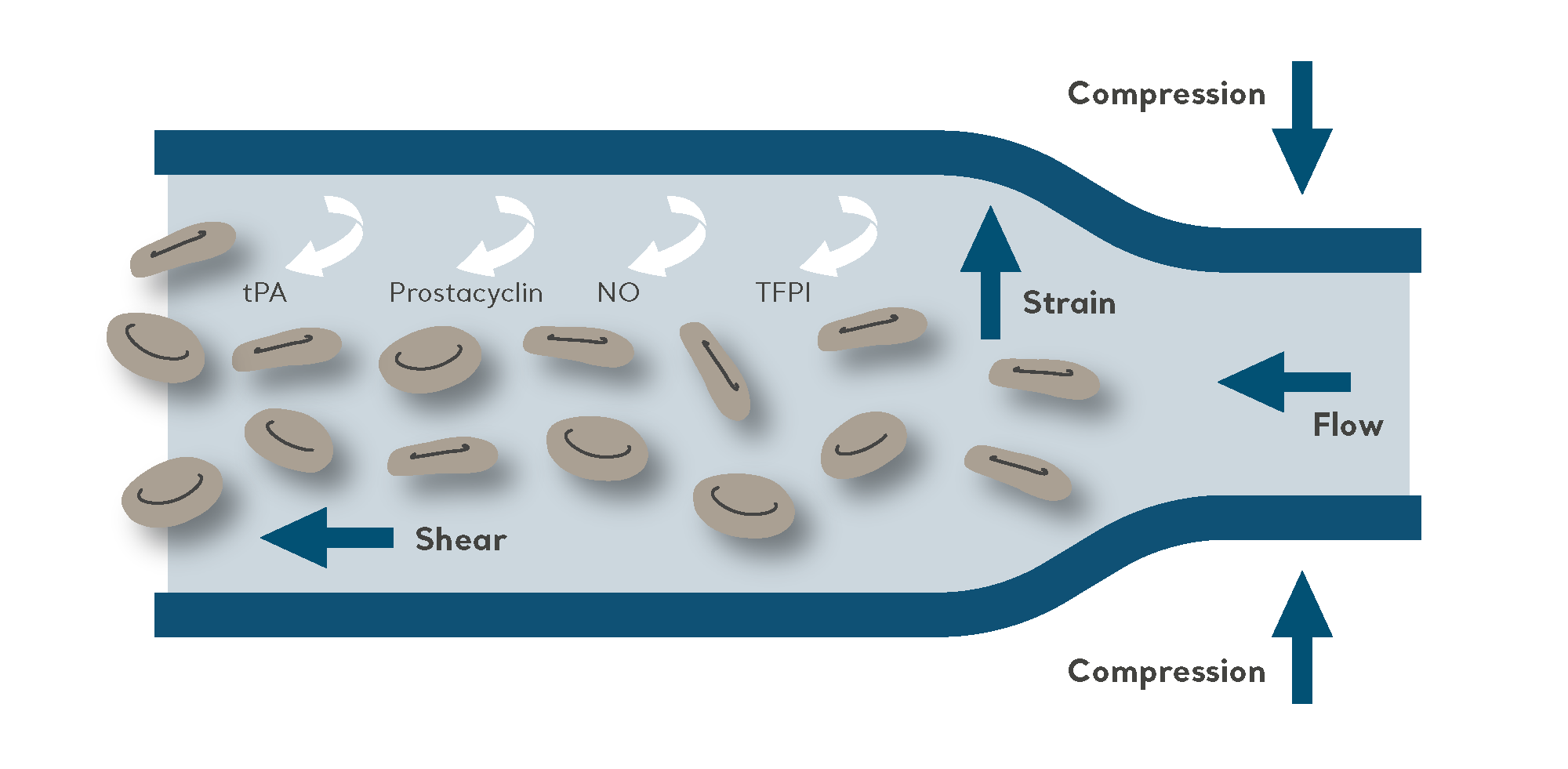
IPC är en icke-invasiv mekanisk metod för VTE-profylax och är effektiv när den används som enda preventivmetod, till exempel för patienter med hög blödningsrisk. Det används också mycket ofta i kombination med farmakologisk profylax till högriskpatienter (för att ytterligare minska risken för VTE).
En betrodd partner för användning av IPC som VTE-prevention
Sedan 1970-talet har VTE-studier tydligt visat fördelarna som behandling med IPC medför. Sedan dess har Arjo varit med och utvecklat lättanvända och kliniskt effektiva IPC-system för att stödja vårdinrättningar över hela världen. Flowtron Active Compression System-serien (ACS) är utformad för att vara bekväm, lättanvänd och kostnadseffektiv.
Arjo strävar också efter att förbättra vårdkvaliteten och hjälpa vårdgivarna att bekämpa djup ventrombos och lungemboli.
”Vårt åtagande handlar om mer än att tillhandahålla pumparna och manschetterna som ingår i vårt Flowtron Active Compression System. Vi vill särskilja Arjo från konkurrenterna genom att vara en partner som tillför service och värdefull kunskap”, säger Henrik Runnerström.
Han fortsätter: ”Även om vårdgivare är medvetna om riskerna kan de sakna tiden, utbildningen och resurserna som krävs för att optimera sina förebyggande strategier. Vår förståelse för dessa svårigheter är det som ligger till grund för att vi har utvecklat våra tjänster och kurser, som är utformade för att stärka vårdgivares kapacitet för att förebygga och behandla VTE.”
Flowtron Active Compression System – en äkta plug-and-play-lösning
Arjos lösning, Flowtron Active Compression System, använder en tryckluftspump för att blåsa upp manschetter runt foten, vaden, låret eller en kombination av dessa.
”Genom att härma vadmuskelns verkningsmekanism ökar IPC blodcirkulationen i de djupa venerna och bidrar till att förhindra blodet från att koagulera. Det är en väletablerad och beprövad behandling med en övertygande evidensbas”, säger Henrik Runnerström.

Flowtron ACS900 (bilden ovan) erbjuder både enhetlig och sekventiell kompression via en mängd olika typer av manschetter. SmartSenseTM Automatic Garment Recognition (bild nedan) kombinerat med enknappsstart gör Flowtron till en smidig plug-and-play-lösning.
”Flexibiliteten minskar behovet av flera pumpmodeller på vårdinrättningen”, säger Henrik. ”Systemet är enkelt att installera och använda och det inbyggda batteriet möjliggör oavbruten behandling även när pumpen inte är ansluten till ett eluttag.”
Han fortsätter: ”Tillsammans med vårt sortiment av manschetter är systemet komfortabelt för vårdtagarna och smidigt för vårdgivarna, och det är mycket effektivt när det gäller intermittent pneumatisk kompression, vilket bidrar till att alla som arbetar med patientvård kan följa behandlingskraven.”
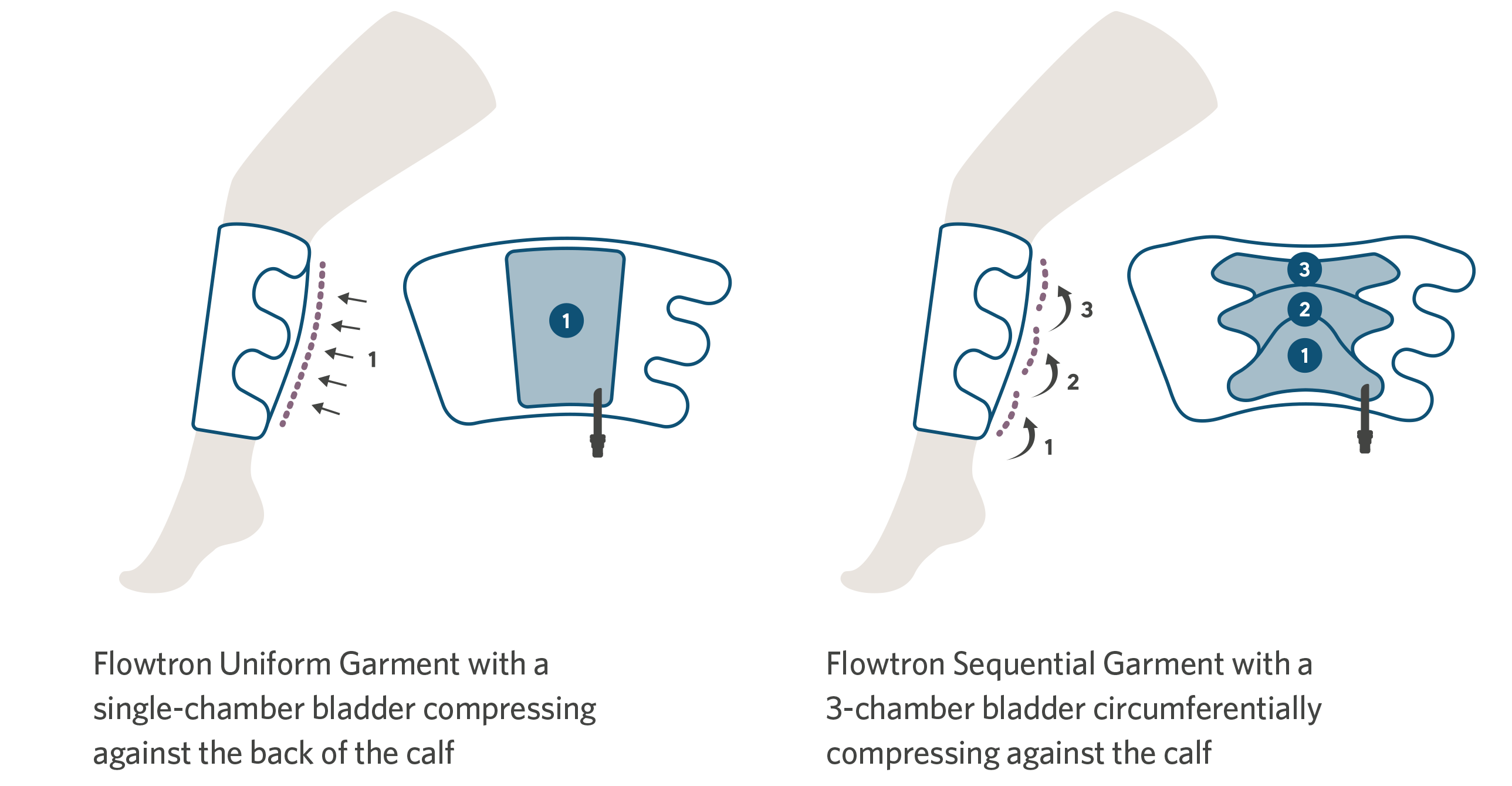
Flowtron-manschetterna finns i olika storlekar, från små till bariatriska, och finns i olika utföranden för vad- och lårlängder som ger antingen sekventiell eller enhetlig kompression. Fotmanschetten finns i normal eller stor fotstorlek. En kombination av olika manschetter kan användas samtidigt. Valet av manschett beror helt och hållet på läkarens önskemål.
Henrik Runnerström förklarar: ”Internationella riktlinjer rekommenderar att behandling sker kontinuerligt i 18–24 timmar per dag8. Studier visar ett direkt samband mellan komfortnivån och patientens vilja att bära manschetter under längre perioder9. Vi strävar efter att förbättra patientkomforten genom att använda material som andas och låter värme och fukt passera igenom, vilket hjälper till att hålla patienten torr och sval.”
Läs mer om Flowtron Active Compression System här
Flowtron IPC – kliniska data
Laboratoriestudier
Många av de inledande undersökningarna som befäste Intermittent Pneumatic Compression som en generisk form av VTE-profylax gjordes med hjälp av föregångarna till dagens Flowtron-serie. Även om tekniken har uppdaterats är de underliggande designprinciperna såsom cykeltryck, inflationshastighet och cykelintervall oförändrade.
Bland de studier som visar den antitrombotiska och profibrinolytiska effekten av IPC finns viktiga fynd som tyder på att IPC minskar sannolikheten för att blodproppar uppstår. IPC bidrar också till att minska risken för koagulering och bryter ned blodproppar när de börjar bildas.7
De viktigaste fynden i dessa studier var att IPC minskar risken för att blodproppar bildas, och att det också hämmar koagulationen och bryter upp blodproppar när de börjar bildas.
Jämförande studier om blodflöde
Omvändning av venös stas är avgörande för prevention, och Flowtron IPC-serien har genomgått ett antal komparativa laboratorietester och genomgående visat fördelaktiga resultat10,11. Se tabellen nedan.
Evidens från laboratoriet
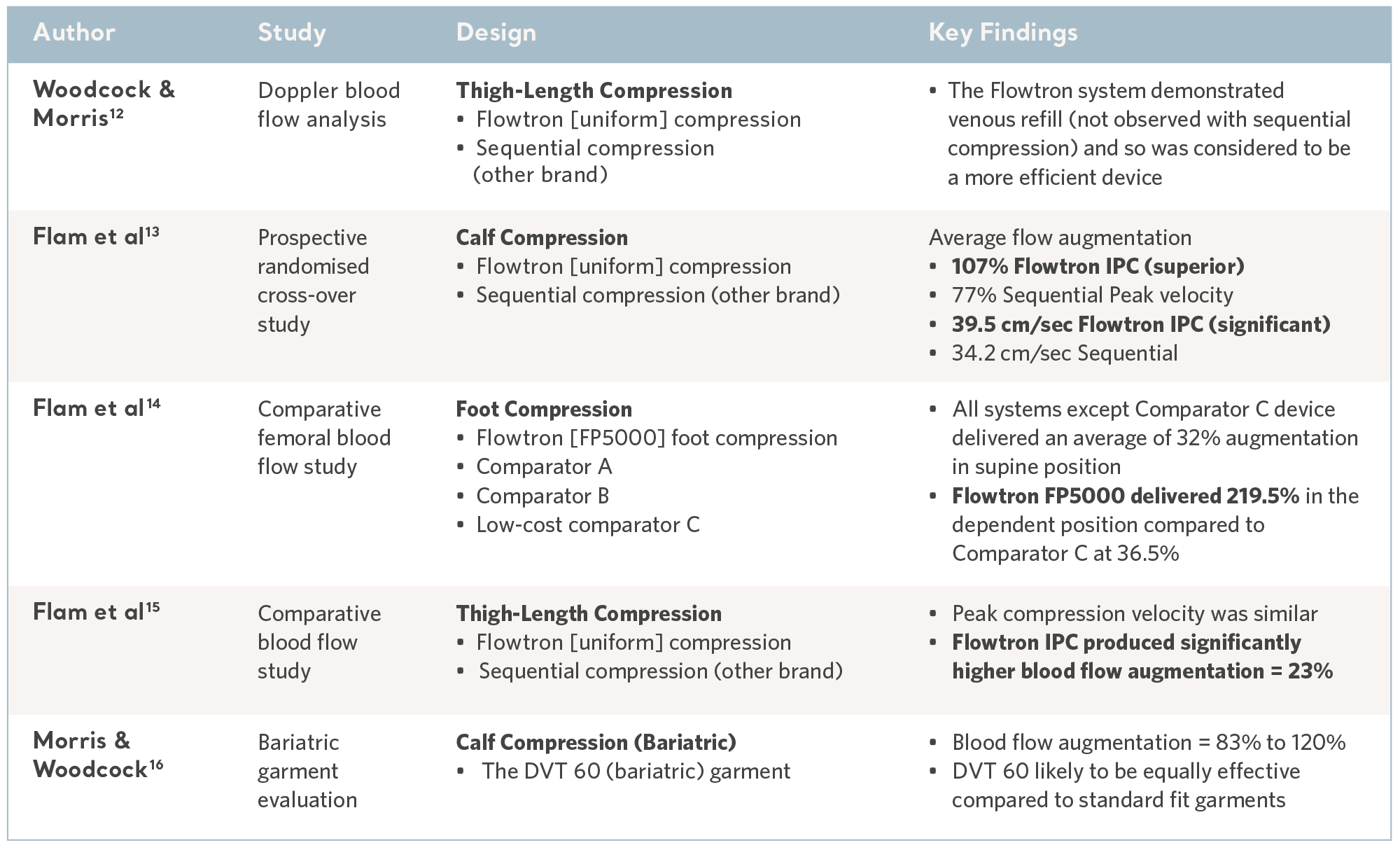
Klinisk effektivitet
Under de senaste 30 åren har oberoende specialister genomfört ett antal kliniska studier. Försökspersonerna har rekryterats från patientpopulationer med högst risk och inom en rad olika kliniska specialområden. Resultaten har genomgående visat att produkterna i Flowtron IPC-sortimentet kan användas profylaktiskt med eller i stället för andra preventiva behandlingsmetoder. Även om IPC nu är allmänt vedertaget som profylax är dessa tidigare undersökningar fortfarande värdefulla17. Se tabellerna nedan.
Kliniska utfallsstudier om Flowtron
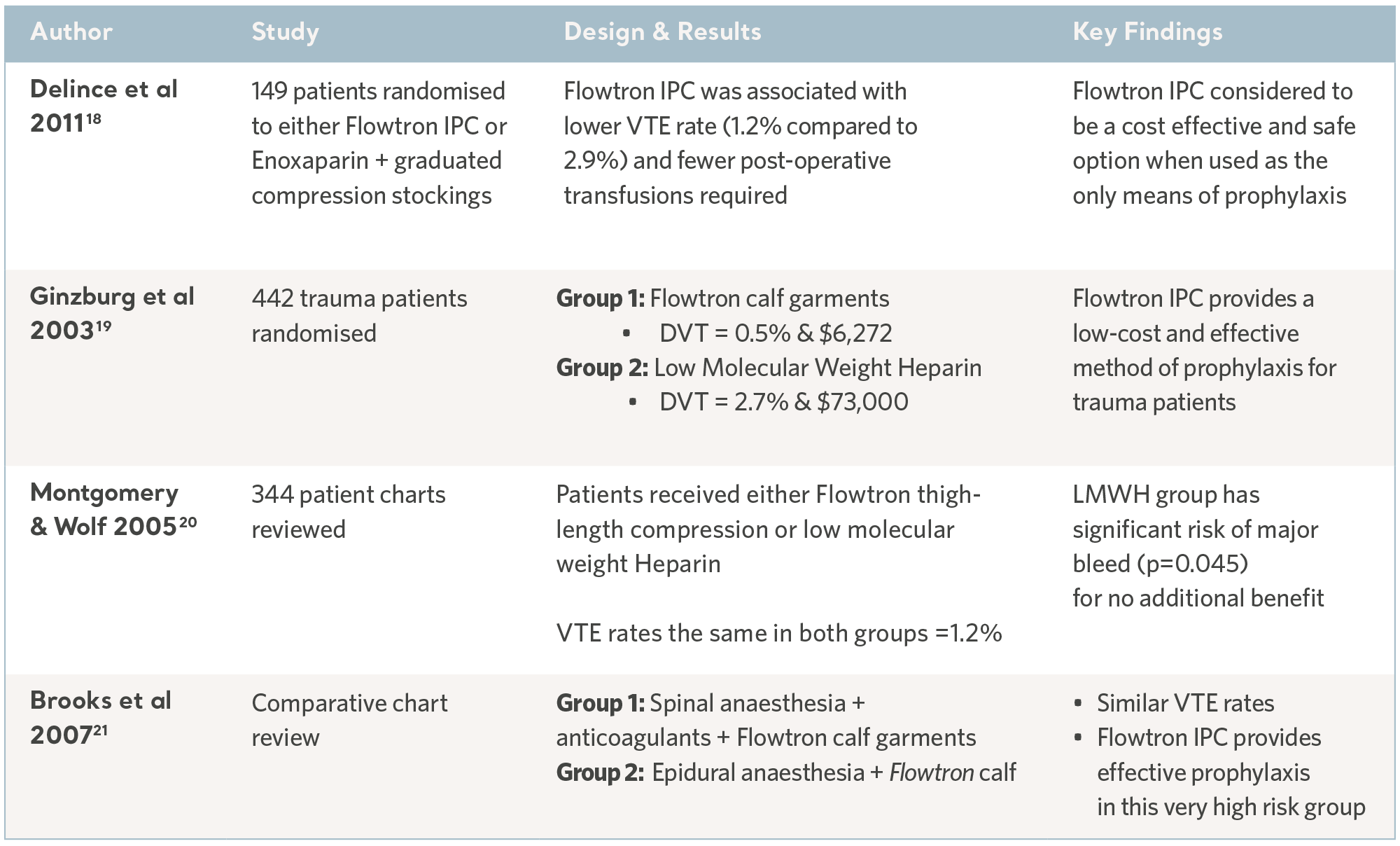
Evidens för Flowtron i specialistgrupper
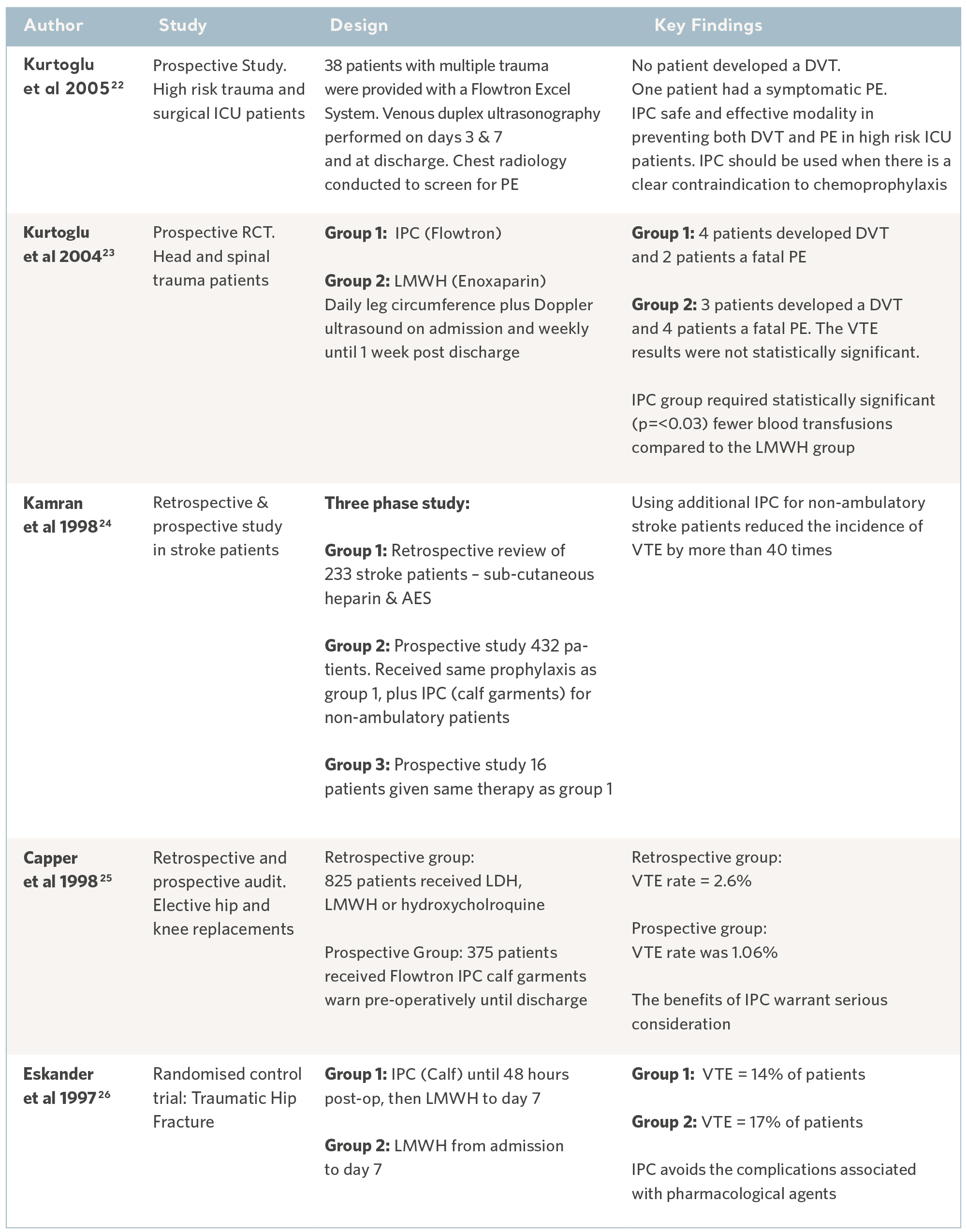
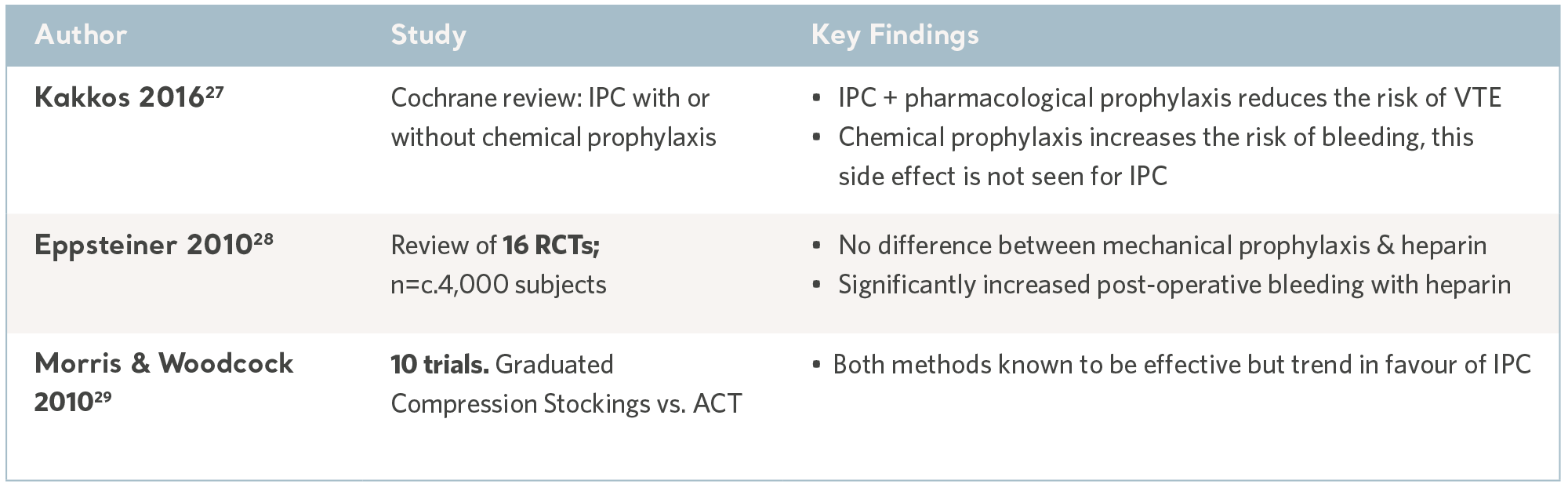
Evidens för IPC från metaanalys och systematiska granskningar
I likhet med alla förebyggande interventioner är IPC endast effektivt om det används med rätt patient vid rätt tidpunkt, och det innebär att man identifierar patienter som är i riskzonen innan en VTE-incident inträffar.
Samtidigt måste risken för biverkningar beaktas, särskilt risken för blödningar i samband med användning av antikoagulantia.
Metaanalyser och systematiska granskningar, där flera evidenskällor kombineras för att fastställa IPC:s totala kliniska användbarhet, är användbara informationskällor och kan vara vägledande för förskrivningar.
Som en utökning av den systematiska granskningen gör publicering av nationella och internationella riktlinjer för klinisk praxis att robust och modern forskning kan omvandlas till rekommendationer; kunskapsluckor fylls av internationella konsensuspaneler. Även om texterna varierar är rekommendationerna i stort sett oförändrade, och IPC anses som en effektiv och säker intervention i alla rekommendationer. Se tabellen nedan.
Evidens för IPC från systematiska granskningar
Användarvänligt
Liksom alla profylaxmetoder är IPC endast fördelaktigt om det används korrekt och tolereras av de patienter som använder det. Bekvämlighet och användarvänlighet är viktiga faktorer och efterlevnaden av behandlingar kan variera.30
I en hektisk vårdmiljö använder sig enheten av ett intuitivt användargränssnitt och lämpliga säkerhetsfunktioner för att risken för skador ska minimeras. Vissa av dessa aspekter har utvärderats i användbarhetstester, och genom oberoende teknikutvärderingar. Utöver kostnadseffektivitet omfattar detta faktorer som bland annat säkerhet, kvalitet och användarvänlighet. Se tabellen nedan.
Bevis från användbarhetsstudier 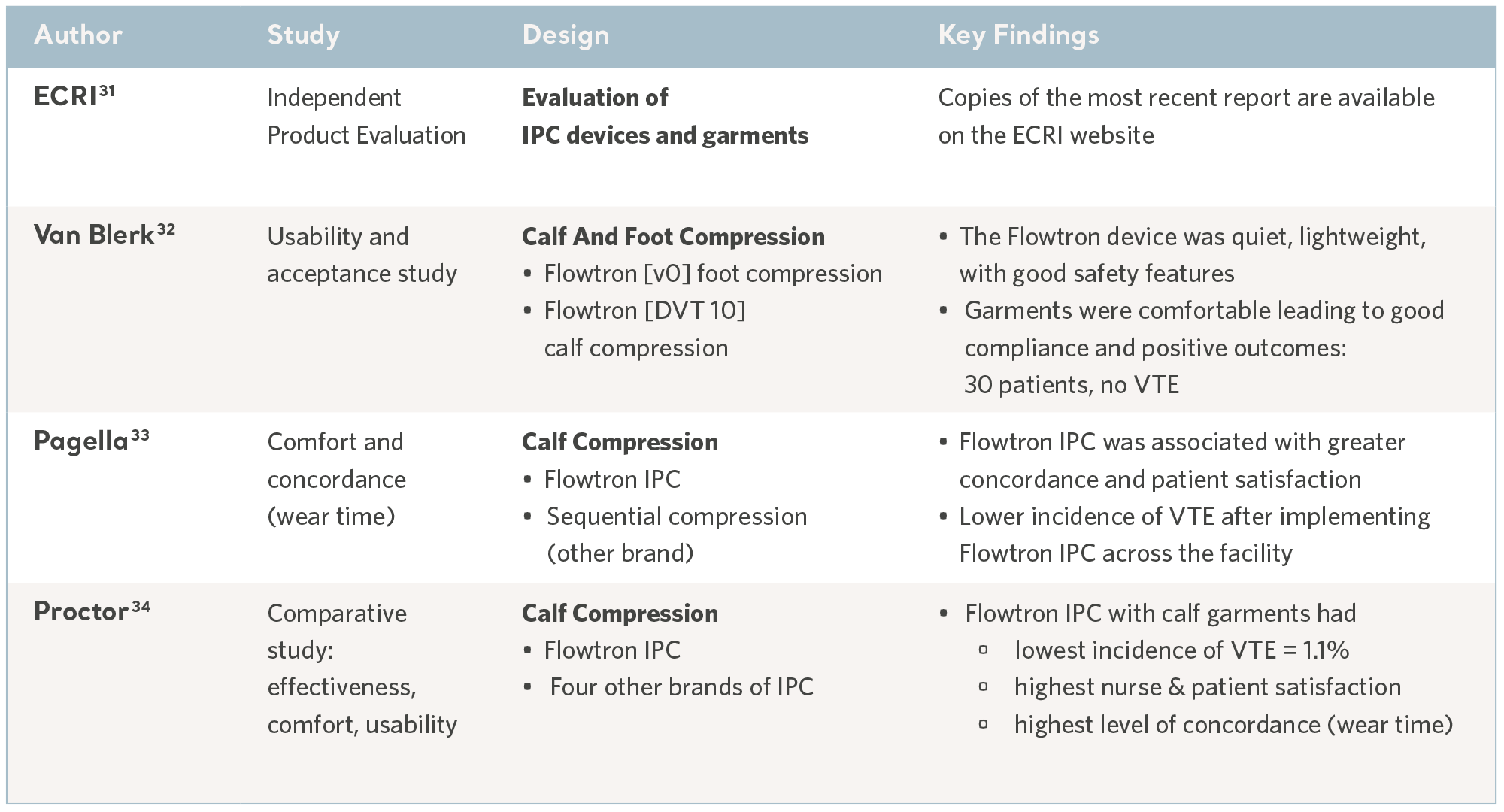
Läs mer om kliniska data om Flowtron IPC
Referenser
1- Beckman MG, Hooper WC, Critchley SE et al. Venous thromboembolism: a public health concern. Am J Prev Med. 2010; 38(4): S495-501.
2- Nelzen O, Bergqvist D, Lindhagen A. Leg ulcer etiology - a cross sectional population study. J Vasc Surg. 1991; 14: 557–64 citerat i Nicolaides A, Fareed J, Kakkar A et al. Prevention and treatment of venous thromboembolism - International Consensus Statement. International Angiology. 2013; 32(2): 111-260.
3- Ruppert A, Steinle T, Lees M. Economic burden of venous thromboembolism: a systematic review. J Med Econ. 2011; 14(1): 65-74
4- Prevention and treatment of venous thromboembolism. Heart.org. https://www.heart.org/en/health-topics/venous-thromboembolism/prevention-andtreatmentof-venous-thromboembolism-vte. Last accessed December 2019.
5- Jha AK, Larizgoitia I, Audera-Lopez C et al. The global burden of unsafe medical care: analytic modelling of observational studies. BMJ Qual Saf 2013; 22: 809-15.
6- Reitsma PH, Versteeg HH, Middeldorp S. Mechanistic view of risk factors for venous thromboembolism. Arteriosclerosis, thrombosis and vascular biology. 2012; 32(3): 563-8.
7- Nicolaides A, Fareed J, Kakkar A et al. Prevention and treatment of venous thromboembolism - International Consensus Statement. International Angiology. 2013;32(2): 111-260.
8- Guyatt GH, AKL EA, Crowther M et al. Executive summary: Antithrombotic Therapy and Prevention of Thrombosis, 9th edition: American College of Chest Physicians. Evidence-Based Clinical Practice Guidelines. Chest. 2012; 141(2):7S-47S.
9- Pagella P, Cipolle M, Sacco E et al. A randomised trial to evaluate compliance in terms of patient comfort and satisfaction of two pneumatic compression devices. Orthop Nurs. 2007; 26(3):169-74.
10- Morris RJ, Giddings JC, Ralis HM, et aL. Haematological and haemodynamic comparison of the Kendall AV Impulse™ and the Arjo [Huntleigh] FP5000 Intermittent Pneumatic Foot Compression System. Arjo Clinical Report 2003.
11- Westrich G, Specht LM, Sharrock NE et al. Venous haemodynamics after total knee arthroplasty: evaluation of active dorsal to plantar flexion and several mechanical compression devices. The Journal of Bone & Joint Surgery. 1998; 80B(6): 1057-1066.
12- WoodcockJPandMorrisRJ.TheeffectoftheKendallSCDTMandArjo[Huntleigh]DVT30 garments on femoral and popliteal vein blood flow measurements. Arjo Clinical Report. 2002.
13- Flam E, Berry S, Coyle A et al. Blood flow augmentation of intermittent pneumatic compression systems used for the prevention of deep vein thrombosis prior to surgery. The American Journal of Surgery. 1996; 171(3): 312-315.
14- Flam E, Nackman G, Tarantino D et al. Intermittent pneumatic compression devices of the foot: a comparison of various systems on femoral vein blood flow velocity augmentation in the v supine and dependent, non-weight bearing positions. Arjo Clinical Report 2000.
15- Flam E, Berry S, Coyle A et al. DVT-profylax: comparison of two thigh high intermittent pneumatic compression systems. Presented at the meeting of the American College of Surgeons, San Francisco. 1993.
16- Morris RJ and Woodcock JP. Intermittent pneumatic compression for bariatric patients – the DVT60 compression garment. Arjo Clinical Report 2003.
17- Falck-Ytter Y, Francis CW, Johanson NA et al. Antithrombotic Therapy and Prevention of Thrombosis, 9th edition: ACCP Evidence Based Clinical Practice Guidelines: Prevention of VTE in Orthopedic Surgery Patients. Chest. 2012; 141: S2.
18- Delince P. RCT of intermittent pneumatic compression (IPC) versus low molecular weight heparin (LMWH) plus anti-embolic stockings (AES) in the prevention of venous thromboembolism during elective hip and knee surgery. Am. Ass. Orth. Surg. Conference 2011.
19- Ginzburg E, Cohn S, Lopez J et al. Randomised clinical trial of intermittent pneumatic compression and low molecular weight heparin in trauma. British Journal of Surgery. 2003; 90: 1338- 1344.
20- Montgomery JS and Wolf JS (2005). Venous Thrombosis Prophylaxis for Urological Laparoscopy: Fractionated Heparin versus Sequential Compression Devices. The Journal of Urology. 2005; 173: 1623-1626.
21- Brooks PJ, Keramati M, Wickline A . Thromboembolism in patients undergoing total knee arthroplasty with epidural analgesia. Journal of Arthroplasty. 2007; 22(5): 641-643.
22- Kurtoglu M, Guloglu R, Ertekin C et al. Intermittent pneumatic compression in the prevention of venous thromboembolism in high-risk trauma and surgical ICU patients. Turkish Journal of Trauma & Emergency Surgery. 2005; 11(1): 38-42.
23- Kurtoglu M, Yanar H et al. Venous thromboembolism prophylaxis after head and
spinal trauma: Intermittent pneumatic compression devices versus low molecular weight heparin. World Journal of Surgery. 2004; 28(8): 807-811.
24- Kamran SI, Downey D and Ruff RL. Pneumatic sequential compression reduces the risk of deep vein thrombosis in stroke patients. Neurology. 1998; 50(6): 1683- 1688.
25- Capper C. External pneumatic compression therapy for DVT prophylaxis. British Journal of Nursing. 1998; 7(14): 851-854.
26- Eskander M, Limb D, Stone M et al. Sequential mechanical and pharmacological thrombo prophylaxis in the surgery of hip fractures. International Orthopaedics. 1997; 21: 259-261.
27- KakkosSK, Caprini JA, Geroulakos G, et al.Combined intermittent pneumatic leg compression and pharmacological prophylaxis for prevention of venous thromboembolism. Cochrane Database of Systematic Reviews. Wiley & Sonds. 2016; 9. www.cochranelibrary.com
28- Eppsteiner RW, Shin JJ, Johnson J, van Dam RM. Mechanical compression versus heparin therapy in postoperative and post trauma patients: a systematic review and meta-analysis. World Journal of Surgery. 2010; 34(1): 10-19.
29- Morris RJ, Woodcock JP. Intermittent pneumatic compression or graduated compression stockings for deep vein thrombosis prophylaxis? A systematic review of direct clinical comparisons. Annals of Surgery. 2010; 251(3): 393-6.
30- Elpern E, Killeen K, Patel G, Senecal PA. Original Research: The Application of Intermittent Pneumatic Compression Devices for Thromboprophylaxis. AJN The American Journal of Nursing. 2013 Apr 1;113(4):30-6
31- ECRI Institute. Mars 2017 https://www.ecri.org/Pages/default.aspx
32- Van Blerk D. Evaluating an Intermittent Compression System for Thromboembolism Prophylaxis. Professional Nurse. 2004; 20(4): 48-49.
33- Pagella P, Cipolle M, Sacco E et al. A randomised trial to evaluate compliance in terms of patient comfort and satisfaction of two pneumatic compression devices.
Orthopaedic Nursing. 2007; 26(3): 169-174.
34- Proctor MC, Greenfield LJ, Wakefield TW et al. A clinical comparison of pneumatic compression devices: the basis for selection. Journal of Vascular Surgery. 2001; 34(3): 459-464.