La importancia de la terapia de compresión en la prevención del TEV
Cuando nos hacemos una pequeña herida, solemos elogiar la capacidad de nuestra sangre para coagular y proteger la herida y evitar una mayor pérdida de sangre. Sin embargo, cuando la sangre comienza a coagularse en el lugar equivocado y el momento inadecuado, las consecuencias pueden cambiarnos la vida, llegando incluso a ser mortales. Cada año, los coágulos de sangre en las venas profundas causan mucho sufrimiento a millones de personas. En este artículo analizamos en profundidad los coágulos de sangre, sus causas y cómo el sistema de compresión activa Flowtron puede ayudar a prevenir esta afección.
«Se estima que hay diez millones de casos de tromboembolismo venoso (TEV) al año en todo el mundo. Se trata de una afección potencialmente mortal que puede suponer un coste significativo para los proveedores de cuidados intensivos y los sistemas sanitarios», afirma Henrik Runnerström, director global de Gestión de Categorías de Productos y Prevención del TEV de Arjo.
Alrededor del 30 % de los pacientes morirá durante los 30 días posteriores al desarrollo del TEV, mientras que el 25 % de las muertes inesperadas de pacientes hospitalizados se diagnostican con embolia pulmonar en la autopsia1.
Alrededor de un tercio de los pacientes con trombosis venosa profunda (TVP) desarrolla síndrome postrombótico, una afección que causa sufrimiento, hinchazón y dolor1. En el 25 % de estos pacientes2, la úlcera crónica resultante se asocia con un coste sustancial del tratamiento en curso3.
Henrik continúa: «Además de todo el sufrimiento humano, el elevado número de casos de TEV se traduce en una carga económica significativa para los proveedores de cuidados intensivos y los sistemas sanitarios».
¿Qué es el TEV?
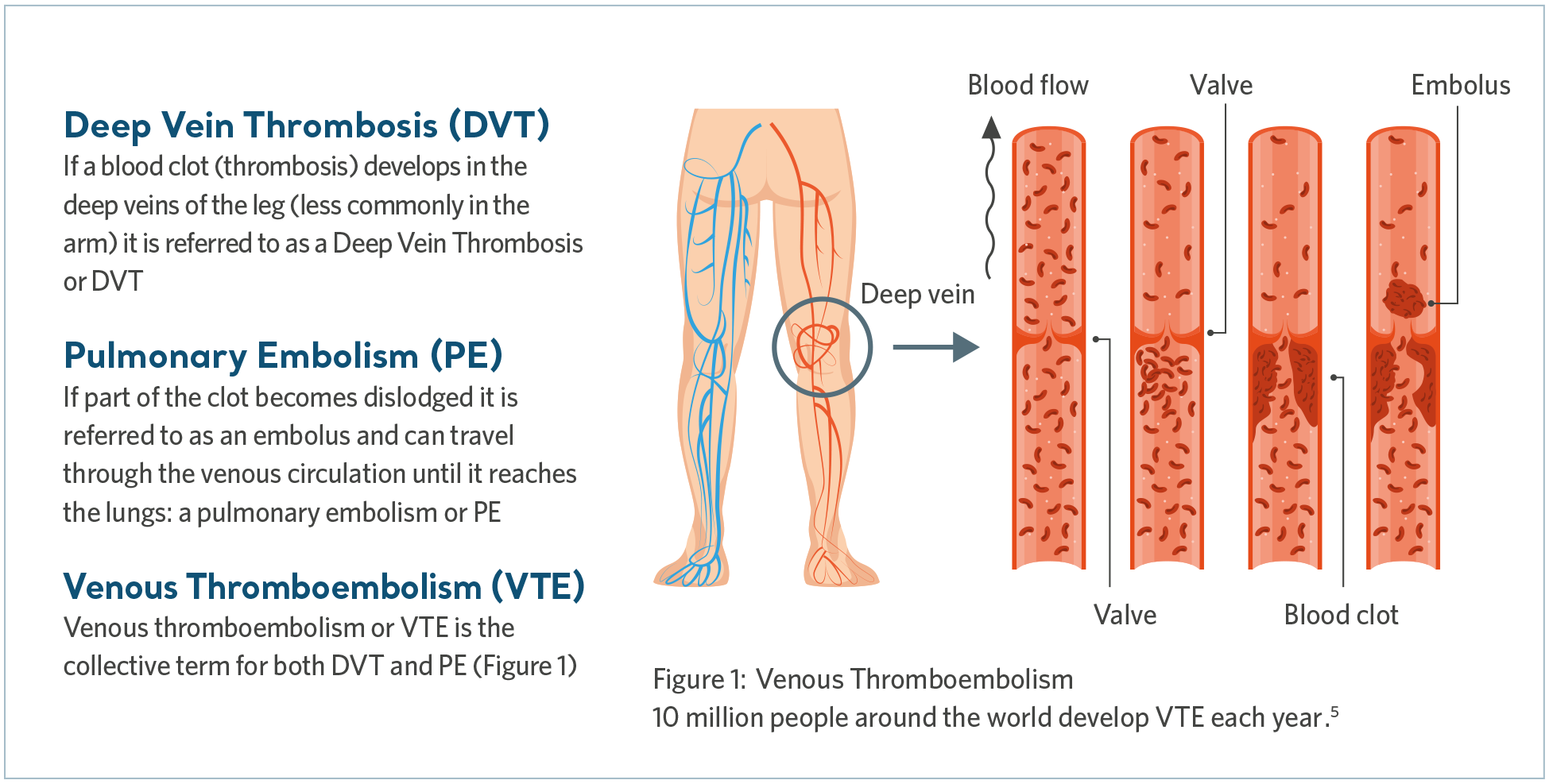
El tromboembolismo venoso (TEV) es el término colectivo que incluye la trombosis venosa profunda (TVP) y la embolia pulmonar (EP). La TVP se produce cuando se forma un coágulo en una vena profunda, normalmente en la pierna, y puede producirse una EP si el coágulo se libera y viaja a los pulmones, bloqueando parte o la totalidad del suministro de sangre.
La embolia pulmonar es una afección potencialmente mortal4. Si bien el diagnóstico y el tratamiento tempranos del TEV pueden conducir a la recuperación, las complicaciones a largo plazo pueden dar lugar a un tratamiento y un sufrimiento de por vida.
¿Qué provoca el TEV?
El TEV se desencadena cuando varios factores de riesgo, conocidos colectivamente como la «tríada de Virchow», inclinan el equilibrio de la homeostasis, que conduce a la formación de coágulos6. Veamos qué tres elementos componen la tríada de Virchow.
La tríada de Virchow
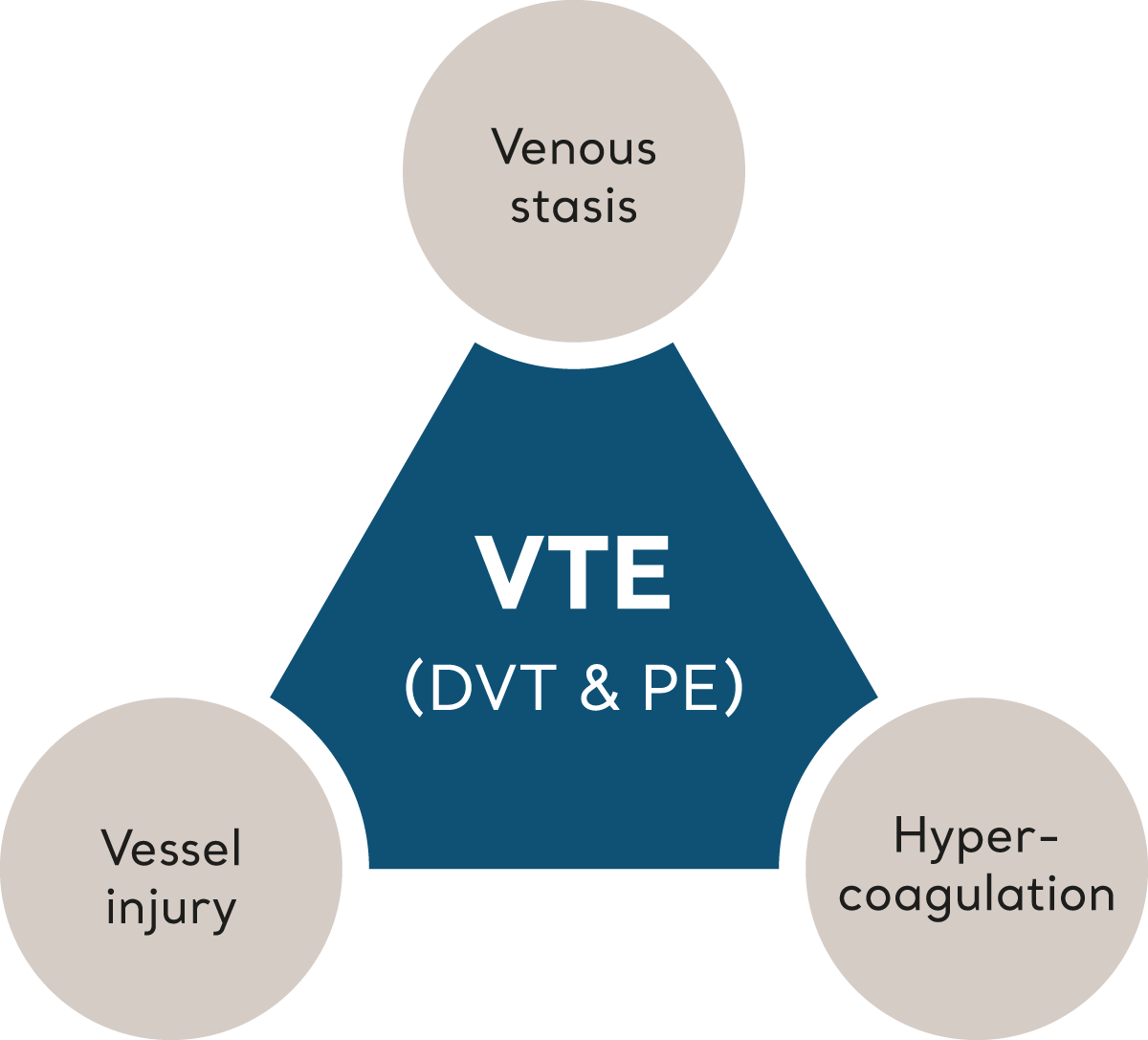
Estasis venosa
Las circunstancias que provocan que el flujo sanguíneo se ralentice (estasis) en las venas profundas aumentarán el riesgo de TEV. La inmovilidad, posiblemente debido a la edad, la fragilidad o el reposo en cama prescrito, es un claro factor de riesgo.
La obstrucción física de los vasos profundos, ya sea debido a fuerzas externas o a la presión de los tumores y los ganglios linfáticos, también está implicada, al igual que las TVP anteriores.
Hipercoagulación
Los cambios en la densidad de la sangre y la química pueden aumentar la tendencia a la coagulación de la sangre. Esto se asocia con afecciones tales como deshidratación simple a hipoxia, neoplasia maligna, traumatismo, terapia hormonal, enfermedad inflamatoria sistémica y predisposición genética.
Lesión de vasos
Pueden producirse lesiones por traumatismo accidental o por intervenciones médicas como procedimientos quirúrgicos o invasivos. Cuando se produce una lesión, una serie de acontecimientos fisiológicos normales inician la adhesión plaquetaria y la formación eventual de un coágulo de sangre; este mecanismo protector sella el daño e inicia el proceso de curación. Sin embargo, a veces este proceso es exagerado o inapropiado.
¿Quiénes tienen riesgo de sufrir una TVP?
Los pacientes quirúrgicos hospitalizados son un grupo de riesgo particular7, ya que la propia cirugía supone el mayor aumento de riesgo, debido a la anestesia (hipercoagulabilidad), los relajantes musculares (estasis) y la intervención quirúrgica
(daños en los vasos). También se sabe que los pacientes hospitalarios no quirúrgicos tienen un alto riesgo de TEV.
Henrik Runnerström comenta: «Hay numerosos factores que contribuyen al TEV, y a pesar de que la afección se suela asociar con personas inmóviles y de edad avanzada, también puede darse en personas aparentemente sanas, en forma y atléticas».
El antiguo jugador profesional de hockey Stefan Elvenes, de Suecia, es un buen ejemplo de ello. Unos meses después de retirarse del hockey sobre hielo, tras 22 años de carrera al más alto nivel en Suecia y Dinamarca, notó una hinchazón en la parte posterior de la pierna izquierda.
«Cuando el médico me dijo que era un coágulo de sangre no podía creerlo. Solo tenía 37 años y estaba en plena forma. A mí no me tocaba tener algo así», comenta Stefan.
Después de saber que las personas jóvenes y atléticas también pueden desarrollar coágulos de sangre, a Stefan se le trató con éxito con anticoagulantes. Sin embargo, tres semanas después de dejar de tomar la medicación, sufrió un grave ataque de pánico.
«En mi cabeza, dejar la medicación significaba un riesgo de que se formara otro coágulo de sangre. Probablemente fuera eso lo que desencadenó mis ataques de pánico», afirma Stefan. «Mi cabeza fue un caos durante mucho tiempo. Pero la terapia constante con un psicólogo me ayudó a dejar atrás los miedos. Ahora lo llevo bien».
Descubre la historia de Stefan aquí
Prevención del TEV
La profilaxis farmacológica, como los anticoagulantes con los que se trató Stefan, es una forma de tratar el TEV. Las estrategias preventivas también implican varios métodos mecánicos, como la compresión neumática intermitente (CNI) y las medias de compresión graduada pasiva (MCG).
La CNI es una intervención muy consolidada y demostrada con una base de pruebas convincente y pocos efectos secundarios, y está indicada para su uso en una amplia variedad de pacientes hospitalizados con riesgo de TEV.
El objetivo de la CNI es impulsar la sangre desde las venas más profundas mediante el inflado y desinflado intermitente de una prenda conectada a una bomba eléctrica.
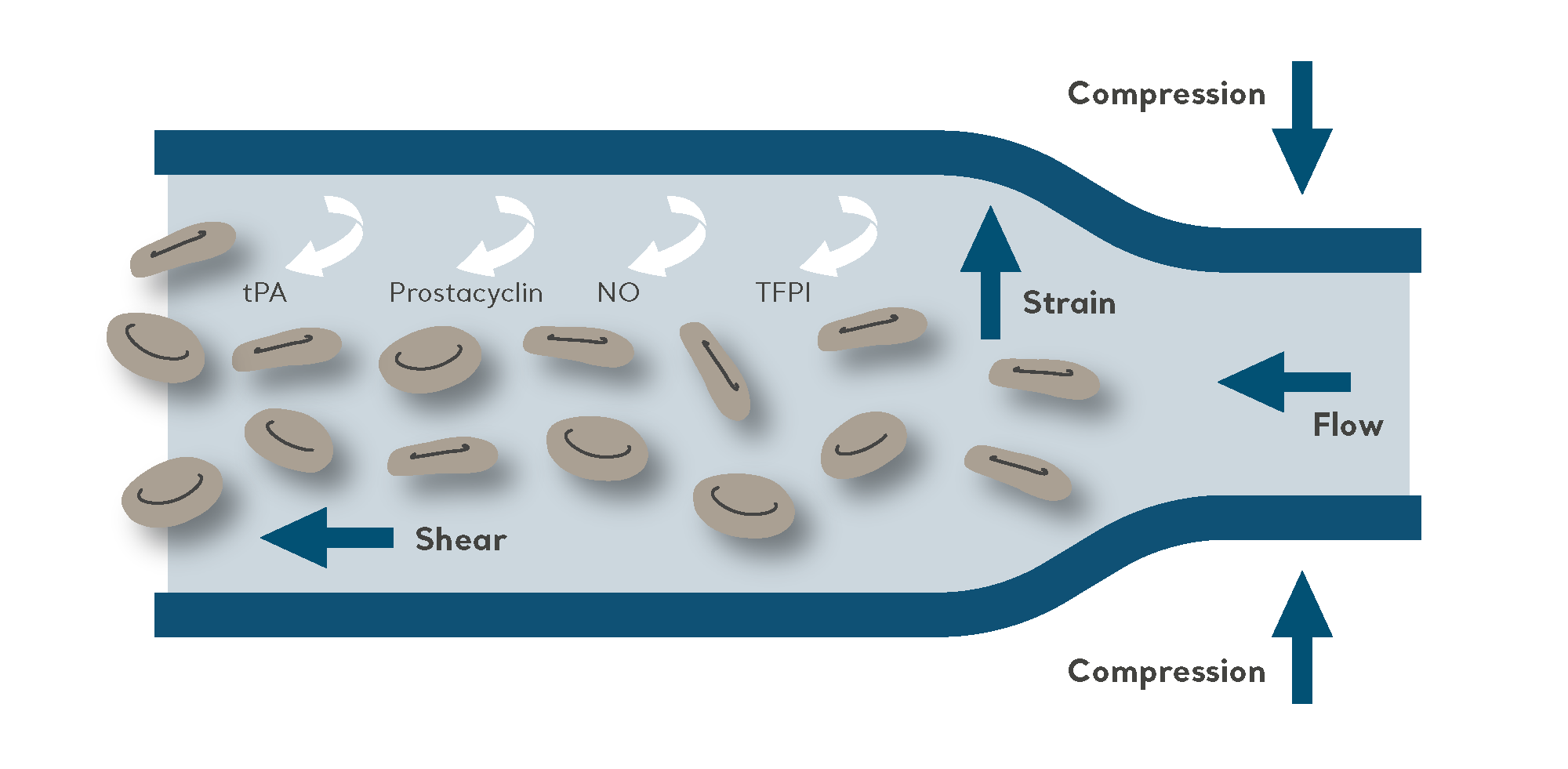
Como método mecánico no invasivo de profilaxis del TEV, la CNI es eficaz cuando se utiliza como única modalidad de prevención, como en el caso de pacientes con un riesgo elevado de sangrado. También se utiliza con mucha frecuencia en combinación con la profilaxis farmacológica para pacientes de alto riesgo (para reducir aún más el riesgo de TEV).
Un socio de confianza para el uso de la CNI en el campo de la prevención del TEV
Desde la década de 1970, los estudios sobre TEV demuestran claramente el beneficio a nivel de protección relacionado con la CNI de las venas profundas de la pierna. Ya desde entonces, Arjo ha tenido un papel decisivo en el desarrollo de sistemas de CNI clínicamente eficaces y fáciles de usar para ayudar a centros de todo el mundo. La gama de sistemas de compresión activa (ACS) Flowtron está diseñada para ofrecer eficacia clínica con comodidad, facilidad de uso y rentabilidad.
Arjo también se dedica a mejorar la calidad de la atención a los pacientes y a ayudar a los profesionales sanitarios a combatir la trombosis venosa profunda y la embolia pulmonar.
«Nuestro compromiso va más allá del suministro de compresores y prendas incluidas en nuestro sistema de compresión activa Flowtron. Queremos diferenciar a Arjo de la competencia siendo un socio que aporta servicios y conocimientos valiosos a su oferta», afirma Henrik Runnerström.
Y continúa: «Aunque los profesionales sanitarios sean conscientes de los riesgos, es posible que carezcan del tiempo, la formación y los recursos necesarios para optimizar sus estrategias de prevención. La comprensión de estos desafíos es la base para desarrollar nuestros servicios y programas de formación, que están diseñados para reforzar la capacidad de prevención y tratamiento del TEV».
Sistema de compresión activa Flowtron: una solución Plug and Play
La solución de Arjo, el sistema de compresión activa Flowtron, utiliza un compresor neumático para inflar prendas alrededor del pie, la pantorrilla, el muslo o una combinación de los tres.
Henrik comenta: «Al imitar la acción de la bomba muscular de la pantorrilla, la CNI mejora la circulación sanguínea en las venas profundas y ayuda a prevenir la coagulación de la sangre. Es un tratamiento muy consolidado y demostrado con una base de pruebas convincente».

El compresor Flowtron ACS900 (imagen anterior) ofrece compresión uniforme y secuencial mediante diferentes tipos de prendas. El reconocimiento automático de prendas SmartSenseTM (imagen inferior), junto con el inicio con un solo botón, convierten a Flowtron en una auténtica solución Plug and Play.
«La flexibilidad reduce la necesidad de diferentes modelos de compresor en un centro sanitario», afirma Henrik. «El sistema es fácil de configurar y utilizar, y la batería integrada permite un tratamiento ininterrumpido incluso cuando el compresor no está conectado a la toma de corriente».
Y prosigue: «En combinación con nuestra gama de prendas, el sistema es cómodo para el paciente, cómodo para el profesional sanitario y clínicamente eficaz a la hora de suministrar compresión neumática intermitente, lo que contribuye a mejorar la conformidad de todos los implicados en la atención al paciente».
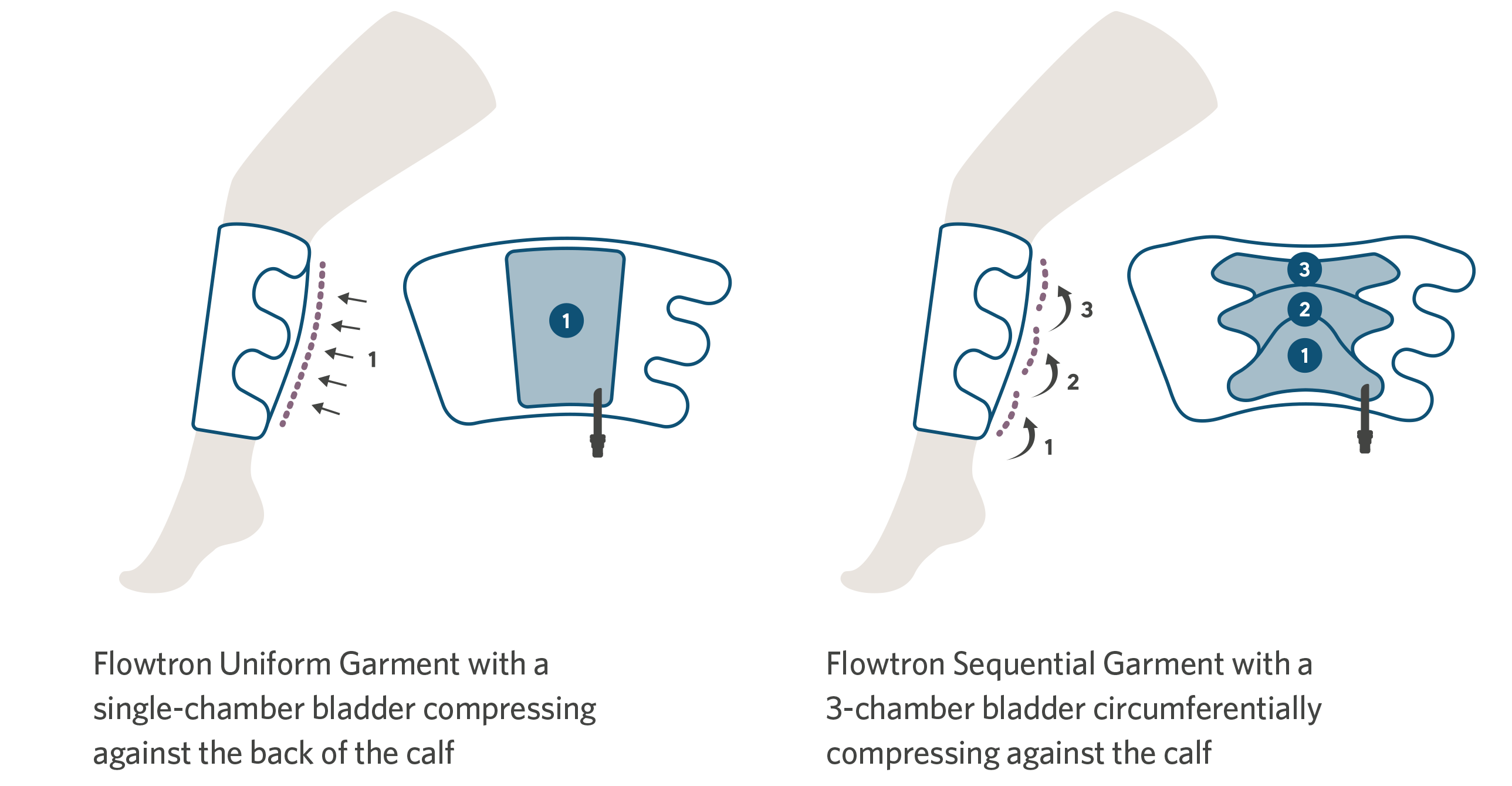
Para mayor comodidad, existe la opción de elegir prendas Flowtron con diferentes longitudes de pantorrilla o muslo, que ofrecen compresión secuencial o uniforme y están disponibles en una amplia variedad de tallas, desde pequeñas hasta bariátricas. La compresión del pie está disponible en tamaño de pie normal o grande. Se puede utilizar una combinación de diferentes prendas simultáneamente. La elección de la prenda depende simplemente de las preferencias del facultativo.
Henrik Runnerström explica: «Las directrices internacionales recomiendan que la terapia se lleve a cabo de forma continua durante 18-24 horas al día8. Los estudios demuestran que existe una conexión directa entre el nivel de comodidad y la disposición de los pacientes a llevar prendas durante periodos más largos9. Nuestro objetivo es mejorar la comodidad del paciente mediante el uso de tejidos transpirables, que ayudan a mantenerlo seco y fresco al permitir la transpiración del calor y la humedad».
Obtenga más información sobre el sistema de compresión activa Flowtron aquí
CNI de Flowtron: datos clínicos
Estudios de laboratorio
Muchos de los primeros estudios de investigación que sustentan la compresión neumática intermitente como forma genérica de profilaxis del TEV se llevaron a cabo utilizando predecesores de la actual gama Flowtron. Si bien la tecnología se ha actualizado, los principios de diseño subyacentes, como la presión del ciclo, la velocidad de inflado y los intervalos de ciclo, siguen siendo los mismos.
Entre los estudios que demuestran el efecto antitrombótico y profibrinolítico de la CNI, los resultados sugieren que la CNI hace que los coágulos tengan menos probabilidades de formarse. Además, la CNI también incrementa la supresión de la formación de coágulos y los descompone cuando empiezan a formarse7.
Los principales hallazgos de estos ensayos fueron que la CNI hace que los coágulos sean menos propensos a formarse, y que también incrementa la supresión de la formación de coágulos y rompe los coágulos cuando comienzan a formarse.
Estudios comparativos de flujo sanguíneo
La inversión de la estasis venosa es clave para la prevención y la gama de CNI de Flowtron se ha sometido a una serie de pruebas comparativas de laboratorio y ha demostrado tener sistemáticamente resultados favorables10,11. Consulte la tabla siguiente.
Pruebas de laboratorio
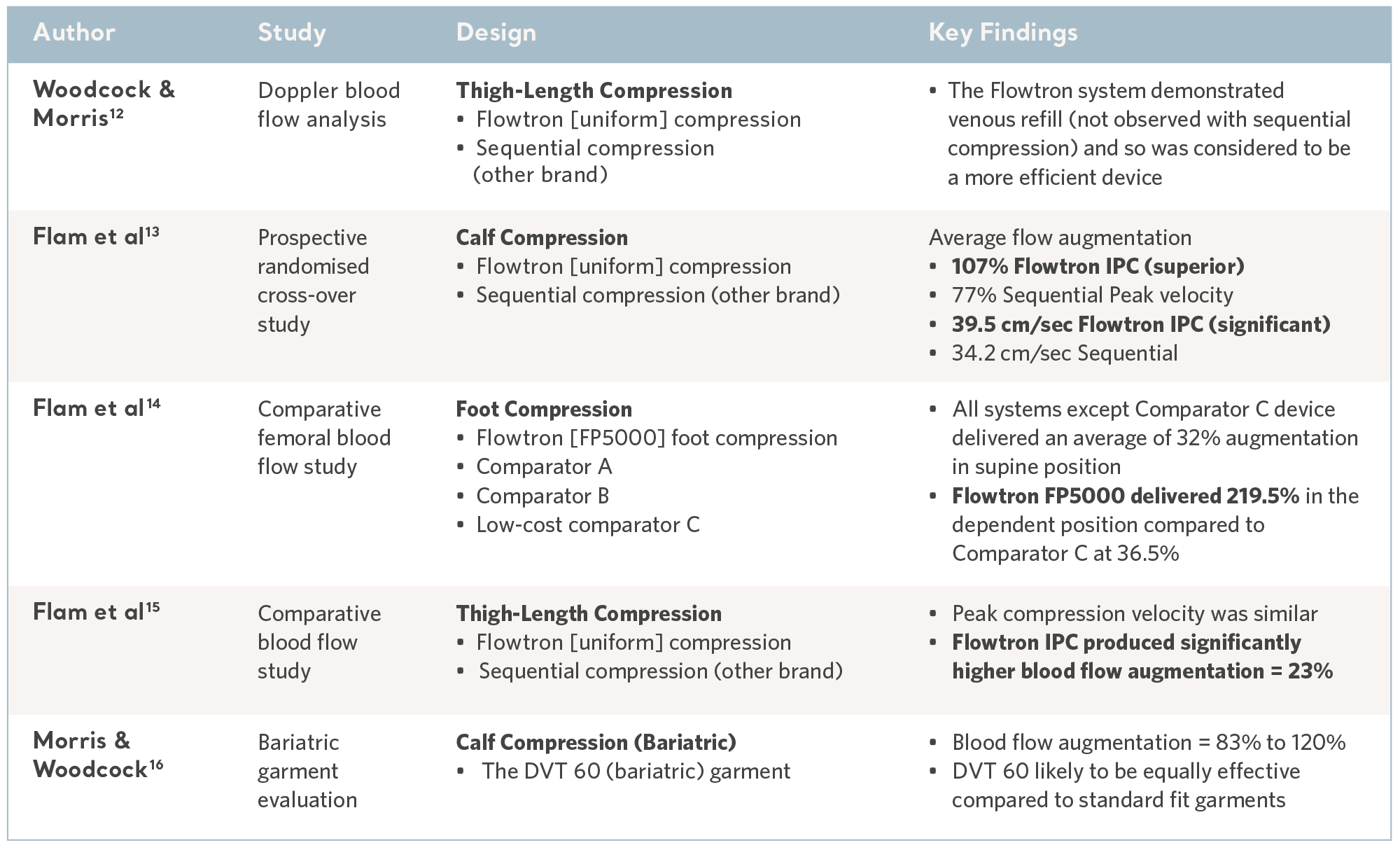
Eficacia clínica
En los últimos 30 años, especialistas independientes han llevado a cabo una serie de estudios clínicos. Se han seleccionado sujetos de las poblaciones de pacientes de mayor riesgo y de una amplia variedad de especialidades clínicas. Los resultados han demostrado sistemáticamente la capacidad profiláctica de la gama de CNI de Flowtron cuando se utiliza con, o en lugar de, otros métodos profilácticos. A pesar de que en la actualidad la CNI goza de una amplia aceptación como forma válida de profilaxis, todos estos estudios siguen teniendo un gran valor17. Consulte las siguientes tablas.
Estudios de resultados clínicos de Flowtron
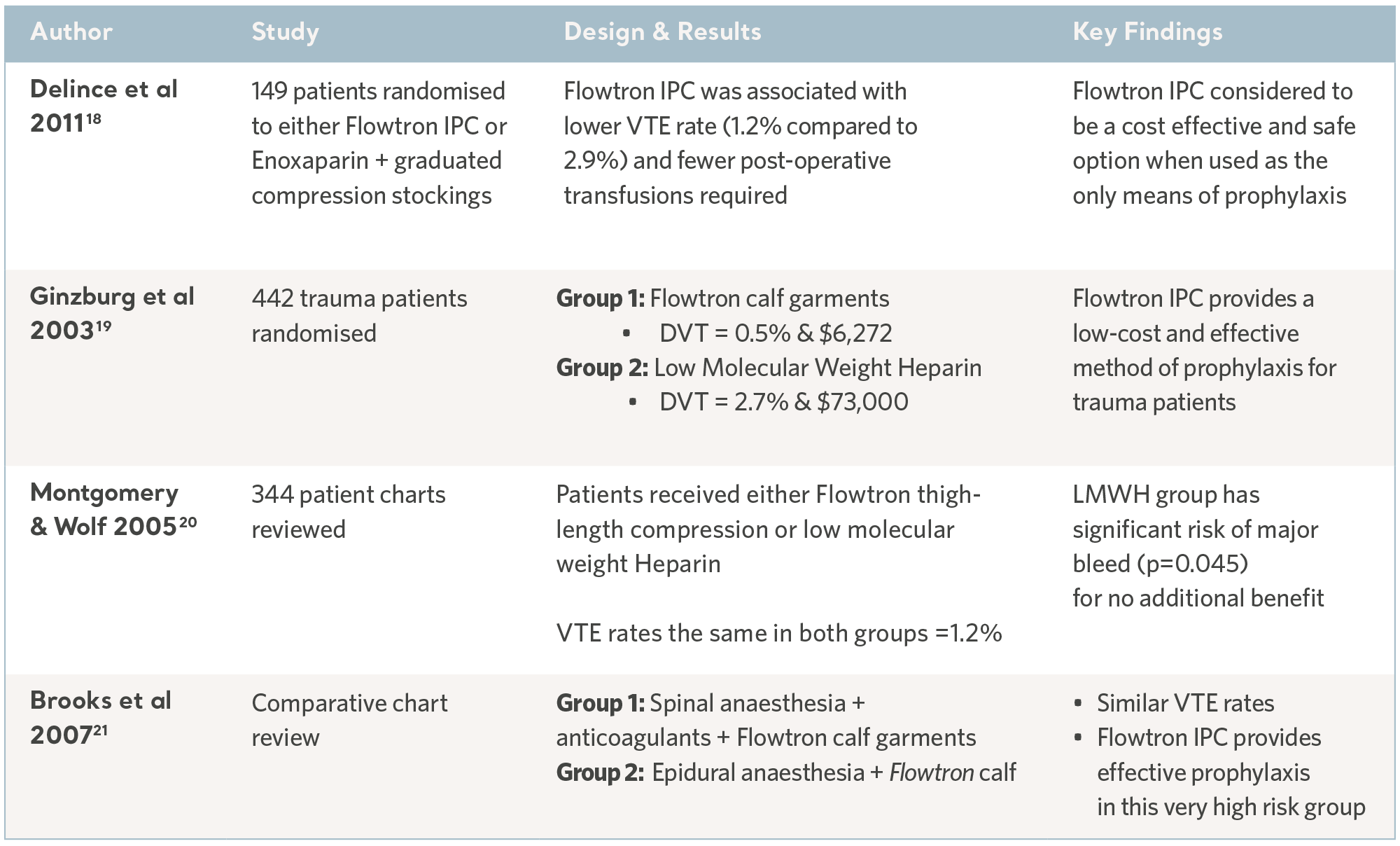
Evidencias de Flowtron en grupos especializados
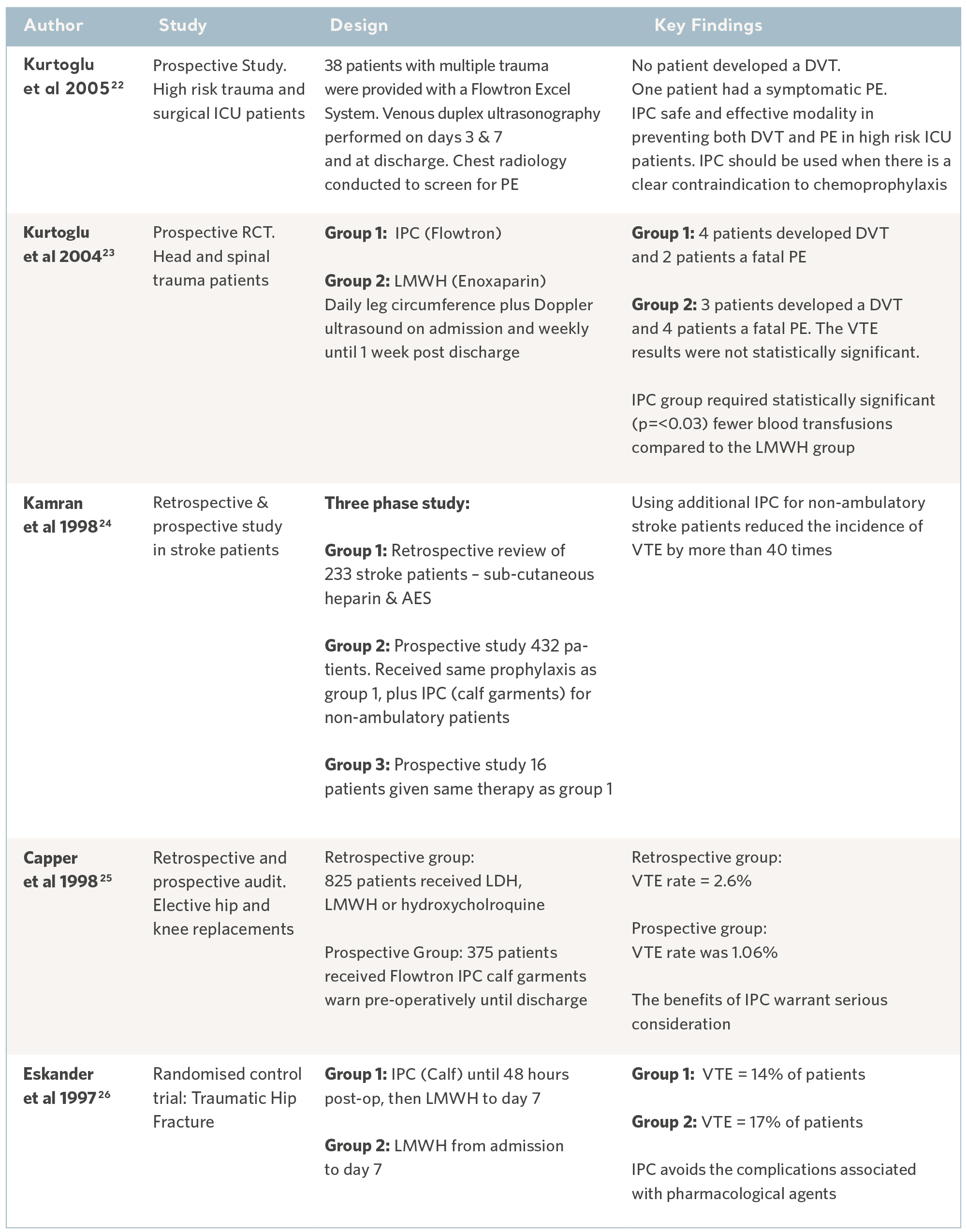
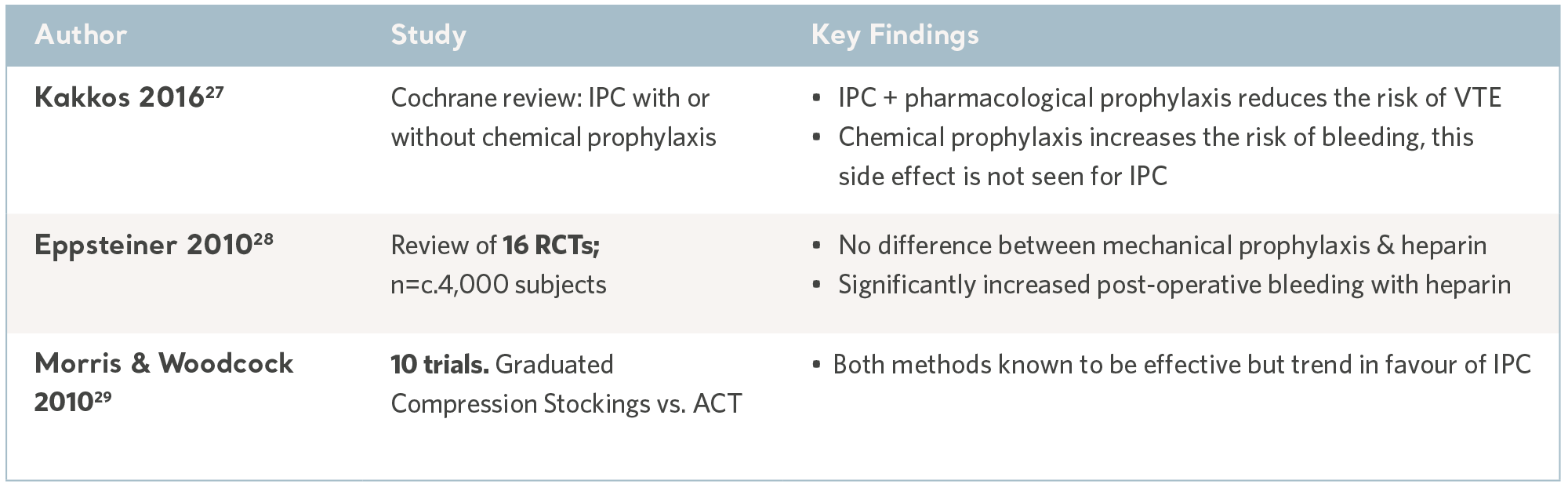
Evidencias de la CNI de metanálisis y revisiones sistemáticas
Al igual que con el resto de intervenciones preventivas, la CNI solo puede ser eficaz si se utiliza con el paciente adecuado en el momento adecuado, y eso significa identificar a los pacientes en riesgo antes de que se produzca un incidente de TEV.
Al mismo tiempo, debe tenerse en cuenta el riesgo de efectos secundarios, en particular el riesgo de hemorragia asociado al uso de anticoagulación.
Los metaanálisis y las revisiones sistemáticas, en las que se combinan múltiples fuentes de pruebas para establecer la utilidad clínica general de la CNI, son fuentes de información de gran utilidad y pueden servir de guía para la prescripción.
Como una extensión de la revisión sistemática, la publicación de directrices de práctica clínica nacionales e internacionales traduce la investigación sólida y contemporánea en recomendaciones discretas, mientras que los paneles de consenso internacionales cubren las lagunas de conocimiento. Aunque la redacción varía, las recomendaciones son en gran medida coherentes y todas aceptan la CNI como una acción eficaz y segura. Consulte la tabla siguiente.
Pruebas de CNI de revisiones sistemáticas
Práctica
Al igual que con cualquier método de profilaxis, la CNI solo es beneficiosa cuando se administra correctamente y los pacientes que la utilizan la toleran. La comodidad y la facilidad de uso son consideraciones clave y la concordancia puede variar30.
En un entorno clínico ajetreado, el dispositivo se beneficia de una interfaz de usuario intuitiva y de las funciones de seguridad adecuadas para reducir al mínimo el riesgo de lesiones. Algunos de estos aspectos se han evaluado en pruebas de usabilidad y, mediante evaluaciones tecnológicas independientes, estas características incluyen seguridad, calidad y facilidad de uso, además de rentabilidad. Consulte la tabla siguiente.
Pruebas de los estudios de usabilidad 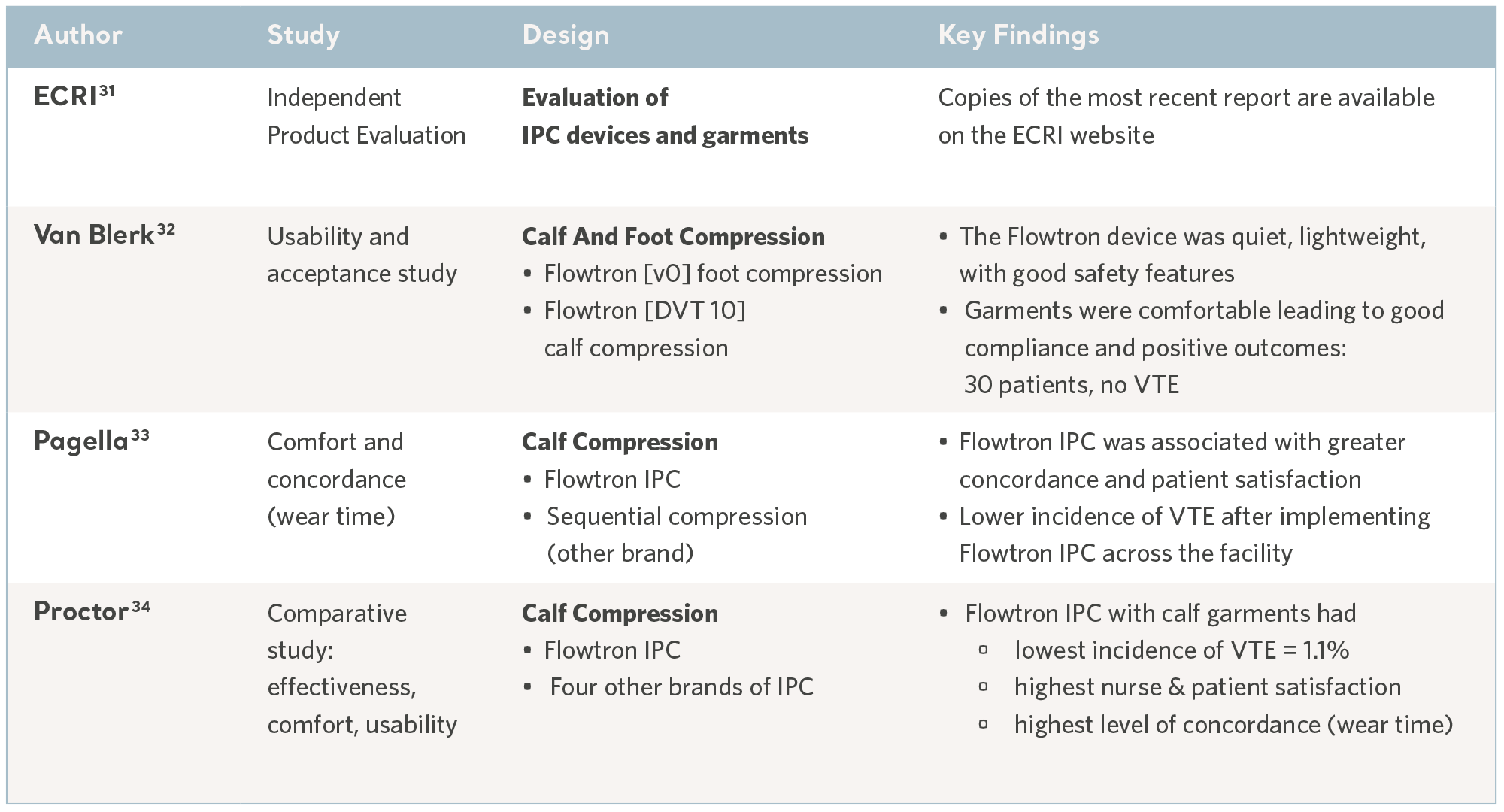
Más información sobre los datos clínicos relacionados con la CNI de Flowtron
Referencias
1- Beckman, M. G.; Hooper, W. C.; Critchley, S. E. et al. Venous thromboembolism: a public health concern. American Journal of Preventive Medicine. 2010; 38(4): S495-501.
2. Nelzen, O.; Bergqvist, D.; Lindhagen, A. Leg ulcer etiology - a cross sectional population study. Journal of Vascular Surgery. 1991; 14: 557-64, citado en Nicolaides, A.; Fareed, J.; Kakkar, A. et al. Prevention and treatment of venous thromboembolism - International Consensus Statement. International Angiology. 2013; 32(2): 111-260.
3. Ruppert, A.; Steinle, T.; Lees, M. Economic burden of venous thromboembolism: a systematic review. Journal of Medical Economics. 2011; 14(1): 65-74.
4. Prevention and treatment of venous thromboembolism. Heart.org. https://www.heart.org/en/health-topics/venous-thromboembolism/prevention-andtreatmentof-venous-thromboembolism-vte. Último acceso: diciembre de 2019.
5. Jha, A. K., Larizgoitia, I., Audera-López, C. et al. The global burden of unsafe medical care: analytic modelling of observational studies. BMJ Quality & Safety. 2013; 22: 809-15.
6. Reitsma, P. H.; Versteeg, H. H.; Middeldorp, S. Mechanistic view of risk factors for venous thromboembolism. Arteriosclerosis, thrombosis and vascular biology. 2012; 32(3): 563-8.
7. Nicolaides, A.; Fareed, J.; Kakkar, A. et al. Prevention and treatment of venous thromboembolism - International Consensus Statement. International Angiology. 2013;32(2): 111-260.
8. Guyatt, G. H.; AKL, E. A.; Crowther, M. et al. Executive Summary: Antithrombotic Therapy and Prevention of Thrombosis. 9th edition. American College of Chest Physicians. Evidence-Based Clinical Practice Guidelines. Chest. 2012; 141(2):7S-47S.
9. Pagella, P.; Cipolle, M.; Sacco, E. et al. A randomised trial to evaluate compliance in terms of patient comfort and satisfaction of two pneumatic compression devices. Orthopaedic Nursing. 2007; 26(3):169-74.
10. Morris, R. J.; Giddings, J. C.; Ralis, H. M. et al. Haematological and haemodynamic comparison of the Kendall AV Impulse™ and the Arjo [Huntleigh] FP5000 Intermittent Pneumatic Foot Compression System. Informe clínico de Arjo de 2003.
11. Westrich, G.; Specht, L. M.; Sharrock, N. E. et al. Venous haemodynamics after total knee arthroplasty: evaluation of active dorsal to plantar flexion and several mechanical compression devices. The Journal of Bone & Joint Surgery. 1998; 80B(6): 1057-1066.
12. Woodcock, J. P. y Morris, R. J. The effect of the Kendall SCDTM and Arjo [Huntleigh] DVT30 garments on femoral and popliteal vein blood flow measurements. Informe clínico de Arjo de 2002.
13. Flam, E.; Berry, S.; Coyle, A. et al. Blood flow augmentation of intermittent pneumatic compression systems used for the prevention of deep vein thrombosis prior to surgery. The American Journal of Surgery. 1996; 171(3): 312-315.
14. Flam, E.; Nackman, G.; Tarantino, D. et al. Intermittent pneumatic compression devices of the foot: a comparison of various systems on femoral vein blood flow velocity augmentation in the v supine and dependent, non-weight bearing positions. Informe clínico de Arjo de 2000.
15. Flam, E.; Berry, S.; Coyle, A. et al. DVT prophylaxis: comparison of two thigh high intermittent pneumatic compression systems. Presentado en la reunión del American College of Surgeons, San Francisco. 1993.
16. Morris, R. J. y Woodcock, J. P. Intermittent pneumatic compression for bariatric patients – the DVT60 compression garment. Informe clínico de Arjo de 2003.
17. Falck-Ytter, Y.; Francis, C. W.; Johanson, N. A. et al. Antithrombotic Therapy and Prevention of Thrombosis, 9th edition: ACCP Evidence Based Clinical Practice Guidelines: Prevention of VTE in Orthopedic Surgery Patients. Chest. 2012; 141: S2.
18. Delince, P. RCT of intermittent pneumatic compression (IPC) versus low molecular weight heparin (LMWH) plus anti-embolic stockings (AES) in the prevention of venous thromboembolism during elective hip and knee surgery. Am. Ass. Orth. Surg. Conferencia de 2011.
19. Ginzburg, E.; Cohn, S.; López, J. et al. Randomised clinical trial of intermittent pneumatic compression and low molecular weight heparin in trauma. British Journal of Surgery. 2003; 90: 1338- 1344.
20. Montgomery, J. S. y Wolf, J. S. (2005). Venous Thrombosis Prophylaxis for Urological Laparoscopy: Fractionated Heparin versus Sequential Compression Devices. The Journal of Urology. 2005; 173: 1623-1626.
21. Brooks, P. J.; Keramati, M.; Wickline, A . Thromboembolism in patients undergoing total knee arthroplasty with epidural analgesia. Journal of Arthroplasty. 2007; 22(5): 641-643.
22. Kurtoglu, M.; Guloglu, R.; Ertekin, C. et al. Intermittent pneumatic compression in the prevention of venous thromboembolism in high-risk trauma and surgical ICU patients. Turkish Journal of Trauma & Emergency Surgery. 2005; 11(1): 38-42.
23. Kurtoglu, M.; Yanar, H. et al. Venous thromboembolism prophylaxis after head and
spinal trauma: Intermittent pneumatic compression devices versus low molecular weight heparin. World Journal of Surgery. 2004; 28(8): 807-811.
24. Kamran, S. I.; Downey, D. y Ruff, R. L. Pneumatic sequential compression reduces the risk of deep vein thrombosis in stroke patients. Neurology. 1998; 50(6): 1683- 1688.
25. Capper, C. External pneumatic compression therapy for DVT prophylaxis. British Journal of Nursing. 1998; 7(14): 851-854.
26. Eskander, M.; Limb, D.; Stone, M. et al. Sequential mechanical and pharmacological thrombo prophylaxis in the surgery of hip fractures. International Orthopaedics. 1997; 21: 259-261.
27. Kakkos, S. K.; Caprini, J. A.; Geroulakos, G. et al. Combined intermittent pneumatic leg compression and pharmacological prophylaxis for prevention of venous thromboembolism. Cochrane Database of Systematic Reviews. Wiley & Sonds. 2016; 9. www.cochranelibrary.com
28. Eppsteiner, R. W.; Shin, J. J.; Johnson, J.; van Dam, R. M. Mechanical compression versus heparin therapy in postoperative and post trauma patients: a systematic review and meta-analysis. World Journal of Surgery. 2010; 34(1): 10-19.
29. Morris, R. J.; Woodcock, J. P. Intermittent pneumatic compression or graduated compression stockings for deep vein thrombosis prophylaxis? A systematic review of direct clinical comparisons. Annals of Surgery. 2010; 251(3): 393-6.
30. Elpern, E.; Killeen, K.; Patel, G.; Senecal, P. A. Original Research: The Application of Intermittent Pneumatic Compression Devices for Thromboprophylaxis. AJN The American Journal of Nursing. 1 de abril de 2013; 113(4):30-6
31. ECRI Institute. Marzo de 2017 https://www.ecri.org/Pages/default.aspx
32. Van Blerk, D. Evaluating an Intermittent Compression System for Thromboembolism Prophylaxis. Professional Nurse. 2004; 20(4): 48-49.
33. Pagella, P.; Cipolle, M.; Sacco, E. et al. A randomised trial to evaluate compliance in terms of patient comfort and satisfaction of two pneumatic compression devices.
Orthopaedic Nursing. 2007; 26(3): 169-174.
34. Proctor, M. C.; Greenfield, L. J.; Wakefield, T. W. et al. A clinical comparison of pneumatic compression devices: the basis for selection. Journal of Vascular Surgery. 2001; 34(3): 459-464.